|
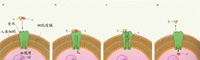 1)外毒素。外毒素由两部分组成,是由两个蛋白质亚基构成的。有毒性的部分为A,是一种酶;与细胞结合的部分叫B,B使外毒素结合到寄主细胞的特定组分上,这个组分多半是酶。 1)外毒素。外毒素由两部分组成,是由两个蛋白质亚基构成的。有毒性的部分为A,是一种酶;与细胞结合的部分叫B,B使外毒素结合到寄主细胞的特定组分上,这个组分多半是酶。
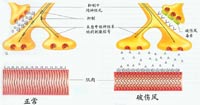 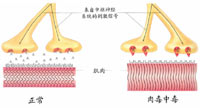
2)内毒素。内毒素是革兰氏阴性菌细胞壁中的一种成分,叫做脂多糖。脂多糖对宿主是有毒性的。内毒素只有当细菌死亡溶解或用人工方法破坏菌细胞后才释放出来,所以叫做内毒素。
内毒素不是蛋白质,因此非常耐热。在100℃的高温下加热1小时也不会被破坏,只有在160℃的温度下加热2到4个小时,或用强碱、强酸或强氧化剂加温煮沸30分钟才能破坏它的生物活性。与外毒素不同之处,还有:内毒素不能被稀甲醛溶液脱去毒性成为类毒素;把内毒素注射到机体内虽可产生一定量的特异免疫产物(称为抗体),但这种抗体抵消内毒素毒性的作用微弱。
内毒素脂多糖分子由菌体特异性多糖、非特异性核心多糖和脂质A三部分构成。脂质A是内毒素的主要毒性组分。不同革兰氏阴性细菌的脂质A结构基本相似。因此,凡是由革兰氏阴性菌引起的感染,虽菌种不一,其内毒素导致的毒性效应大致类同。这些毒性反应主要有:
发热反应。人体对细菌内毒素极为敏感。极微量(1-5纳克/公斤体重)内毒素就能引起体温上升,发热反应持续约4小时后逐渐消退。自然感染时,因革兰氏阴性菌不断生长繁殖,同时伴有陆续死亡、释出内毒素,故发热反应将持续至体内病原菌完全消灭为止。内毒素引起发热反应的原因是内毒素作用于体内的巨噬细胞等,使之产生白细胞介素1、6和肿瘤坏死因子α等细胞因子,这些细胞因子作用于宿主下丘脑的体温调节中枢,促使体温升高发热。
白细胞反应。细菌内毒素进入宿主体内以后,血流中占白细胞总数60-70%的中性粒细胞数量迅速减少,这是因为细胞发生移动并粘附到组织毛细血管上了。不过1-2小时后,由内毒素诱生的中性细胞释放因子刺激骨髓释放其中的中性粒细胞进入血流,使其数量显著增加,有部分不成熟的中性粒细胞也被释放出来。革兰氏阴性菌的伤寒沙门菌是例外,其内毒素使白细胞总数始终是减少状态,目前还不清楚是什么原因。由于绝大多数被革兰氏阴性菌感染的患者血流中白细胞总数都会增加,所以现在医生在诊断前,为了初步区别是细菌性感染还是病毒性感染,常常要化验病人的血液,对白细胞进行总数测定和分类计数。被病毒感染的病人,其白细胞总数和中性粒细胞百分比基本在正常值范围内。
内毒素血症与内毒素休克。当病灶或血流中革兰氏阴性病原菌大量死亡,释放出来的大量内毒素进入血液时,可发生内毒素血症。大量内毒素作用于机体的巨噬细胞、中性粒细胞、内皮细胞、血小板,以及补体系统和凝血系统等,便会产生白细胞介素1、6、8和肿瘤坏死因子α、组胺、5羟色胺、前列腺素、激肽等生物活性物质。这些物质作用于小血管造成功能紊乱而导致微循环障碍,临床表现为微循环衰竭、低血压、缺氧、酸中毒等,于是导致病人休克,这种病理反应叫做内毒素休克。
关于内毒素休克,过去曾有过惨痛的教训。20世纪40年代青毒素刚问世的时候,医生发现青霉素对脑膜炎奈瑟菌引起的流行性脑膜炎疗效非常显著。因此,凡发现这类病人,一律优选青霉素进行治疗;且按照一般规律,用药剂量随病情严重程度而递增。结果发生了意外,用大剂量青霉素治疗重症脑膜炎患者时,不少发生了内毒素休克而死亡。后来经过研究分析,发现了其中的原委。病情严重的患者,体内存在的病原菌数量多,医生采用大剂量“轰炸”,意欲“一举歼敌”。快速、彻底杀灭病原体,这种战略无可非议,但有些医生忽略了另一方面,即流行性脑膜炎的病原菌是属革兰氏阴性菌的脑膜炎奈瑟菌,其致病物质是内毒素,而内毒素是要在病菌死亡后再放出的。如今用大剂量青霉素一下子将全部病菌杀死,也就是使大量内毒素一次放出,促成了内毒素休克,加速了患者的死亡。随着医学的进步,现在医生遇到这类病人,一方面仍然要用大剂量的有效抗菌药物去对付,同时要加用激素类药物,以保护对内毒素敏感的细胞不对内毒素诱生的细胞因子发生反应,从而度过“休克”难关。犹如外科手术时,采用麻醉药使病人丧失痛觉一样。
 某些代表性的内毒素 肉毒毒素的临床应用 某些代表性的内毒素 肉毒毒素的临床应用
|